生物电子系统(如假肢)的构建需要通过使用电极在生物组织和电子设备之间建立连接。对于用于神经界面的电极,应仔细考虑电极材料的电学性能、力学性能和生物相容性。
早期的神经电极是用钨、不锈钢、金、铂等金属制作的单微丝或多微丝,因为它们具有高导电性和生理环境下的化学稳定性。后来,随着微制造技术的进步,研究人员开始使用重掺杂半导体作为电极,如基于硅的微针电极。尽管上述电极提供了合适的获取和刺激神经信号的高空间分辨率、大电流注入,和信噪比(信噪比)以及易于制造等特点,但这些电极的大抗弯刚度比神经组织产生一系列免疫反应,无法长期使用。在生理移位过程中,神经胶质瘢痕和血脑屏障破裂发生在电极表面附近(即,神经组织和附在颅骨上的装置之间总是有相对位移,这可能是由于呼吸和心跳引起的微运动,也可能是由于身体运动引起的大运动)。随后,神经元死亡,胶质细胞(如星形胶质细胞和小胶质细胞)激活,在电极附近形成绝缘层或鞘。在植入后6周内,鞘层变得越来越密集,并抑制了电极附近轴突的再生。因此,电极和神经组织之间的阻抗水平增加,这大大降低了记录过程中的信噪比,阻止了有效的神经刺激。
有几种方法可以减少由于神经电极引起的免疫反应。一种方法是通过涂覆透明质酸或聚乙二醇(PEG)组成的水凝胶来控制探头的疏水性。尽管这些材料已经被证明可以防止电极附近的胶质细胞增生,但随着时间的推移,它们最终被氧化而失效。另一种技术是将生物活性分子或地塞米松等药物与电极表面结合。这些材料被证明可以防止神经元细胞的死亡,或促进电极附近神经元的附着。最近,研究发现在L1或在电极表面生长干细胞可以同时阻止胶质细胞增生和促进神经突的生长。
虽然上述方法工作得很好,但并不能解决神经组织与电极之间固有的弯曲刚度失配问题。弯曲刚度由电极结构的惯性矩和组成材料的弹性模量决定。因此,为了降低弯曲刚度,可以对电极进行几何设计,如减少电极的尺寸,和/或使用低弹性模量的材料。在电极的几何工程中,为了降低弯曲刚度,采用了各种形状的电极,如网格结构和分形基结构。这些形状提供了很高的灵活性,同时允许使用高模量材料,具有更好的信号记录和微加工过程的可用性等优点。对于周围神经系统(PNS)接口,设备的形状对于缓解长期神经刺激和记录的脱髓鞘和神经丢失尤为重要。尽管取得了一定的成功,但单靠电极的几何工程并不能完全解决神经电极的刚性问题。因此,开发低弹性模量的新型软材料是非常必要的。
导电聚合物和碳基材料
导电聚合物具有作为神经电极的巨大潜力。导电聚合物的电化学聚合可使导电材料沉积在具有可调厚度和导电性的各种表面上。在导电聚合物中,聚吡咯(PPy)和PEDOT在神经界面应用方面的研究最为广泛(图1)。在传统的金属电极上使用这种聚合物作为涂层材料也被证明可以降低阻抗和增加信噪比。

碳基材料如碳纳米管和石墨烯也被用于神经电极。例如,基于碳纳米管的电极装置,其电极直径可小至5~ 10µm,且已被证明可降低胶质瘢痕和随后的免疫反应。碳纤维电极电极直接更小(~3 - 5µm)。其他研究人员将石墨烯和氧化石墨烯作为透明电极沉积在平面器件上,可以与光学成像相结合。
含有聚合物、碳、金属或共轭有机纳米颗粒混合物的复合材料已被用于降低电极的硬度,同时保持高导电性。一种常见的复合材料是碳纳米管与聚合物的混合物。碳纳米管也被石墨烯薄片包裹,并沉积在基底上,形成大面积的高导电性软电极。这些碳基复合材料可以像传统的微加工技术一样具有高分辨率。
导电聚合物和碳基材料目前的电性能低于传统的刚性金属或硅基电极。因此,虽然神经活动记录的可行性已经被证明,但它们作为整个电极用于神经刺激目前是有限的。目前,导电聚合物和碳基材料主要用作传统刚性电极的涂层材料,以提高电性能。导电聚合物和碳基材料与神经组织相比也相对较硬(弹性模量约为1 GPa)。为了解决这些挑战,包含导电聚合物和软组分如水凝胶的复合材料正在开发中。
导电水凝胶
水凝胶是高含水量的交联聚合物网络。使用水凝胶的最大优点是它们的机械性能与生物组织的相似。研究表明,涂有软水凝胶的刚性可植入电极可以显著改善生物相容性(减少机械失配),而电性能的变化可以忽略不计。与导电聚合物类似,水凝胶涂料也含有生物活性物质。
导电水凝胶在过去几年引起了广泛的关注。通常,水凝胶是电子绝缘体,然而,通过盐或电子导电元件的掺入,可以分别成为离子或电子导电。离子导电水凝胶由于离子扩散引起的导电性低或稳定性差,通常不适合植入设备。为了解决这些问题,有人开发了含有相分离聚乙二醇和盐的离子导电水凝胶(图2)。在这些水凝胶中,相分离阻止了离子扩散,同时允许增加柔软度和更高的离子导电性。这些离子导体在体内表现出高度的生物相容性。

图2 (左)离子电路原理图,使用离子导电水凝胶。(中)肌肉刺激回路的照片。(右)用各种脉冲信号刺激肌肉。
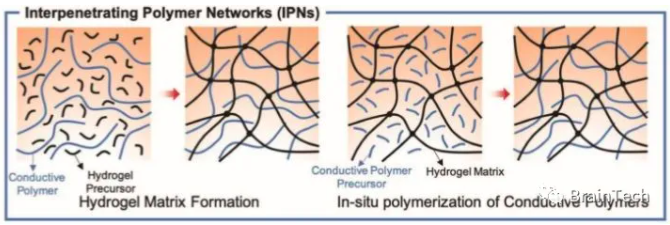
导电水凝胶可以通过添加导电填料如金属纳米颗粒、碳纳米管和石墨烯来实现。导电水凝胶纳米复合材料具有良好的导电性和机械顺应性,在神经电极领域具有广阔的应用前景。除了导电填料,人们可以用导电聚合物合成导电水凝胶。一种水凝胶是交联导电聚合物与支撑水凝胶聚合物网络的混合物,被称为互穿网络水凝胶(IPNs)。目前已报道的导电聚合物IPNs有 PEDOT:PSS、PPy或聚苯胺(PANI)。一般来说,制备IPNs的方法,是将导电组件在支撑水凝胶网络内进行原位聚合,或将导电聚合物与水凝胶前体混合(图3)。虽然由此产生的水凝胶在机械上是符合要求的,但它们在生物电子学中的应用由于其过低的导电性受到阻碍。对此,鲍哲南等人提出了一种潜在的解决方案,他们证明,在含有PEDOT:PSS和聚(丙烯酸)(PAA)的IPNs中,PEDOT:PSS的凝胶化可以建立良好连接的传导通路,从而产生高达23 S m−1的高电导率。更重要的是,可以通过改变PEDOT:PSS和PAA的分子组成来调整这些IPNs的机械性能,而不会对导电性产生任何影响。
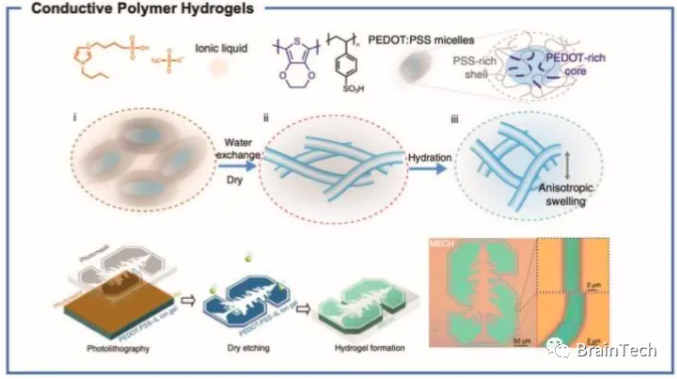
第二种水凝胶本质上是导电的水凝胶,它由不支持聚合物网络的导电聚合物组成,因此比IPNs具有更高的导电性。如图4所示的PEDOT:PSS导电水凝胶电导率为47.4 S cm−1。PEDOT:PSS与离子液体添加剂相互连接,该添加剂在凝胶化后通过水交换除去。得到的PEDOT:PSS水凝胶具有低模量、水稳定性和生物相容性。更重要的是,光刻技术使水凝胶能够模压成复杂的微结构和微柱电极阵列。与氧化铱电极相比,光刻微柱电极阵列具有更高的信噪比和信号振幅。
导电水凝胶因其模量与神经组织模量相近,被认为是替代传统刚性电极用于神经界面的最佳选择。到目前为止,研究主要局限于改善机械和电气性能,而导电水凝胶在生物体内的性能还没有得到充分的探索。因此,需要在体内进行一体化的装置水平的演示,以确定它们的实际可行性。根据最近的报道,尽管导电聚合物具有令人满意的体外性能,但其体内生物相容性较差。同样,导电水凝胶在神经界面的实际应用可能会面临意想不到的挑战。使用导电聚合物和水凝胶的一个优点是它们的性能是可调的;因此,可以添加生物降解性和自愈性等功能。具体来说,使用可生物降解的导体可以避免移除植入设备的不良过程,而机械鲁棒性和长期可靠性可以通过使用自愈合材料和设备来实现。最重要的是,在短期内,研究应该集中在降低这些材料的阻抗,因为它目前还不足以用于神经记录。
参考文献:Jun Chang Yang, Jaewan Mun, Se Young Kwon,Seongjun Park, Zhenan Bao, and Steve Park. Electronic Skin: Recent Progress andFuture Prospects for Skin-Attachable Devices for Health Monitoring, Robotics,and Prosthetics. Adv. Mater. 2019, 1904765.
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。

